Werkpakketten
We hebben 5 werkpakketten ontworpen waarin psychiaters en pathologen (WP1), celbiologen met ruime ervaring in omics-technologieën (WP2) en computationele wetenschappers (WP3) nauw zullen samenwerken met chemici (WP4) en neurobiologen (WP5).
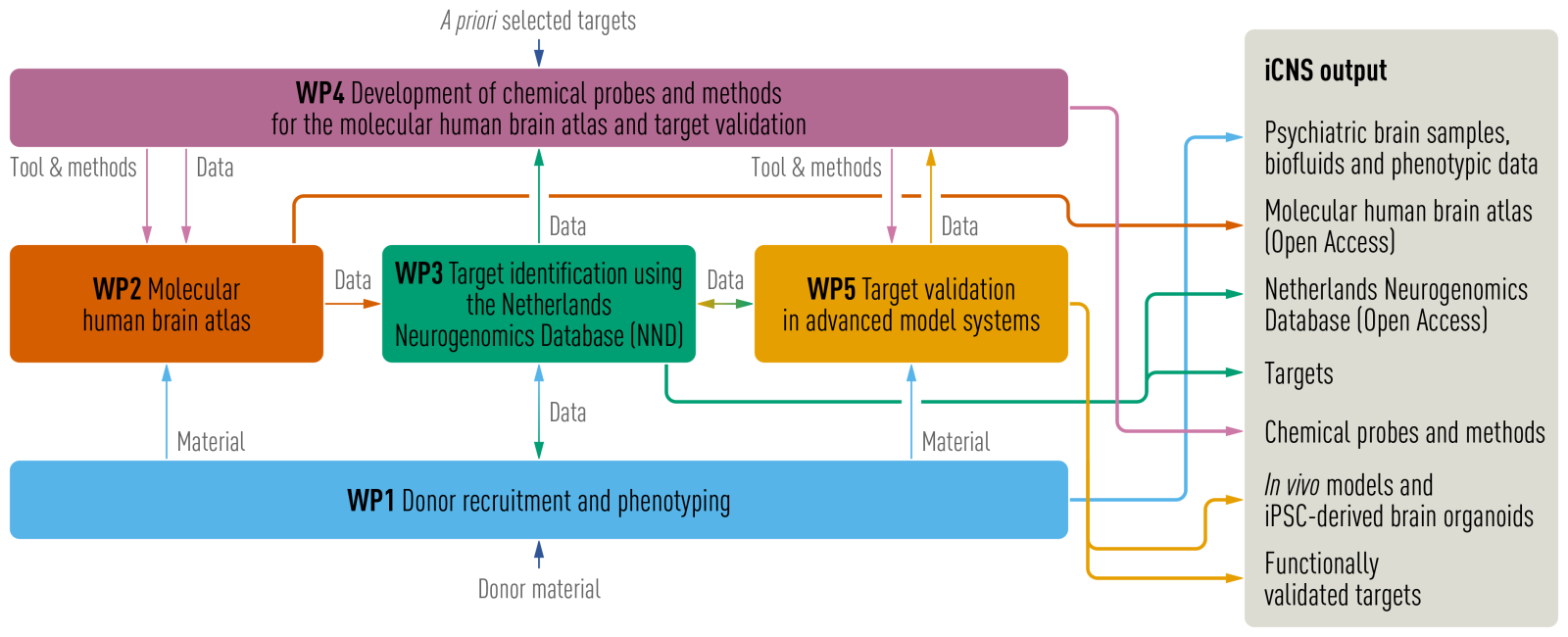
Donorwerving en fenotypering
Leiders: Jörg Hamann en Karel Scheepstra
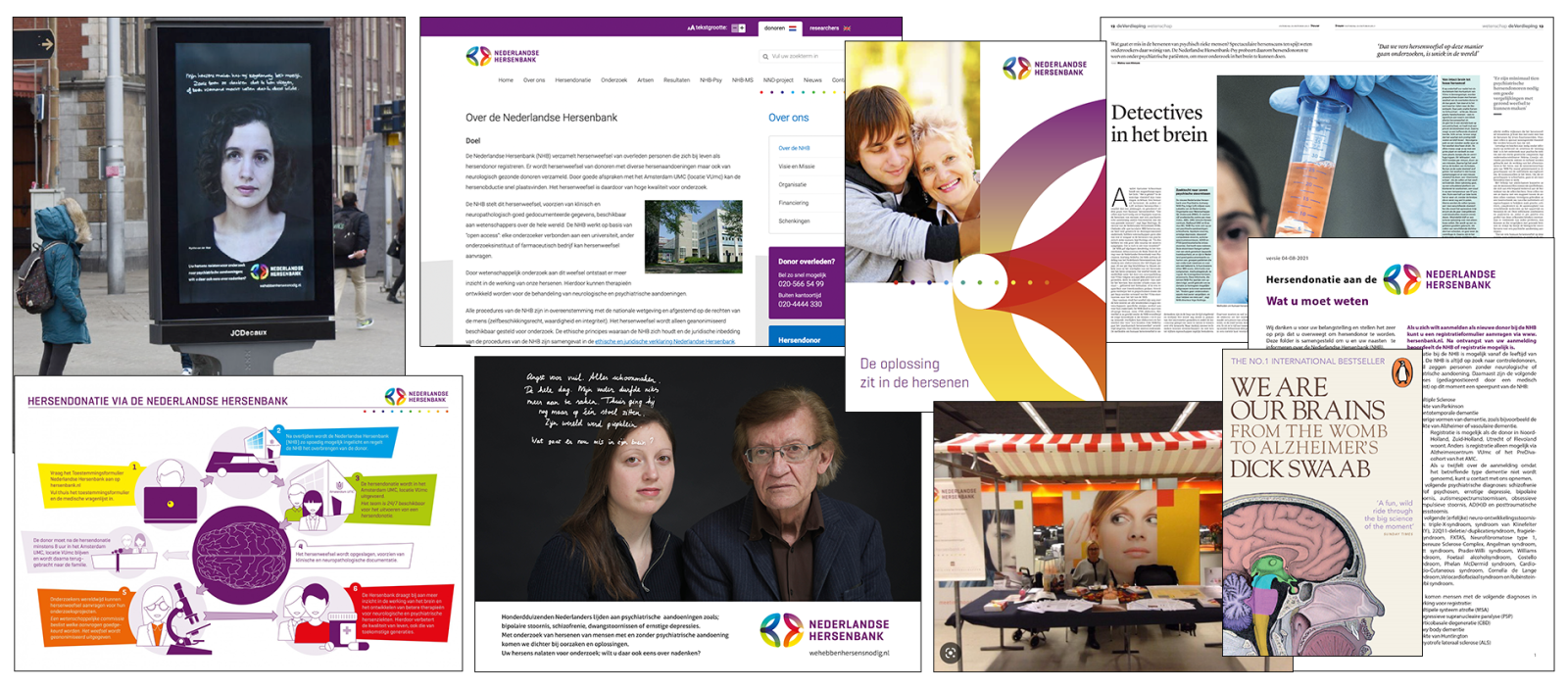
Werkpakket 1 heeft als doel het ondersteunen en aanvullen van het langetermijn hersendonorprogramma van de Nederlandse Hersenbank (NBB). Hiervoor wordt hersenweefsel van goed gekarakteriseerde donoren verzamelt om fundamenteel en translationeel psychiatrisch onderzoek te faciliteren. Het vergaren van hoogwaardig diep-fenogetypeerd hersenmateriaal van patiënten met neuropsychiatrische stoornissen en controlepersonen is van belang voor de internationale onderzoeksgemeenschap en Nederlandse onderzoekers, waaronder het iCNS-consortium.
Werkpakket 1 bouwt voort op het succesvolle NBB-Psy-donorprogramma, gericht op het verzamelen van hersenmonsters en gegevens van donoren met de diagnose ernstige depressie (MDD), schizofrenie (SCZ), bipolaire stoornis (BD), obsessief-compulsieve stoornis (OCD), posttraumatische stressstoornis (PTSD), autistische spectrumstoornis (ASS), aandachtstekortstoornis met hyperactiviteit (ADHD) en controles. Deze bestaande, landelijke infrastructuur gaan we versterken en uitbreiden met een biobank die hersenvocht en bloed verzamelt van patiënten met psychiatrische stoornissen. Deze activiteiten zullen moleculair psychiatrisch onderzoek binnen iCNS en toekomstige open-access verspreiding onder onderzoekers wereldwijd mogelijk maken. Het iCNS zal nieuwe normen stellen op het gebied van hersenbankieren door verder te gaan dan klinische diagnoses. Klinische en pathologische heterogeniteit zullen kunnen worden opgenomen in gestandaardiseerde beoordelingen.
Moleculaire hersenatlas van het menselijk brein
Leiders: Lot de Witte en Bart Eggen
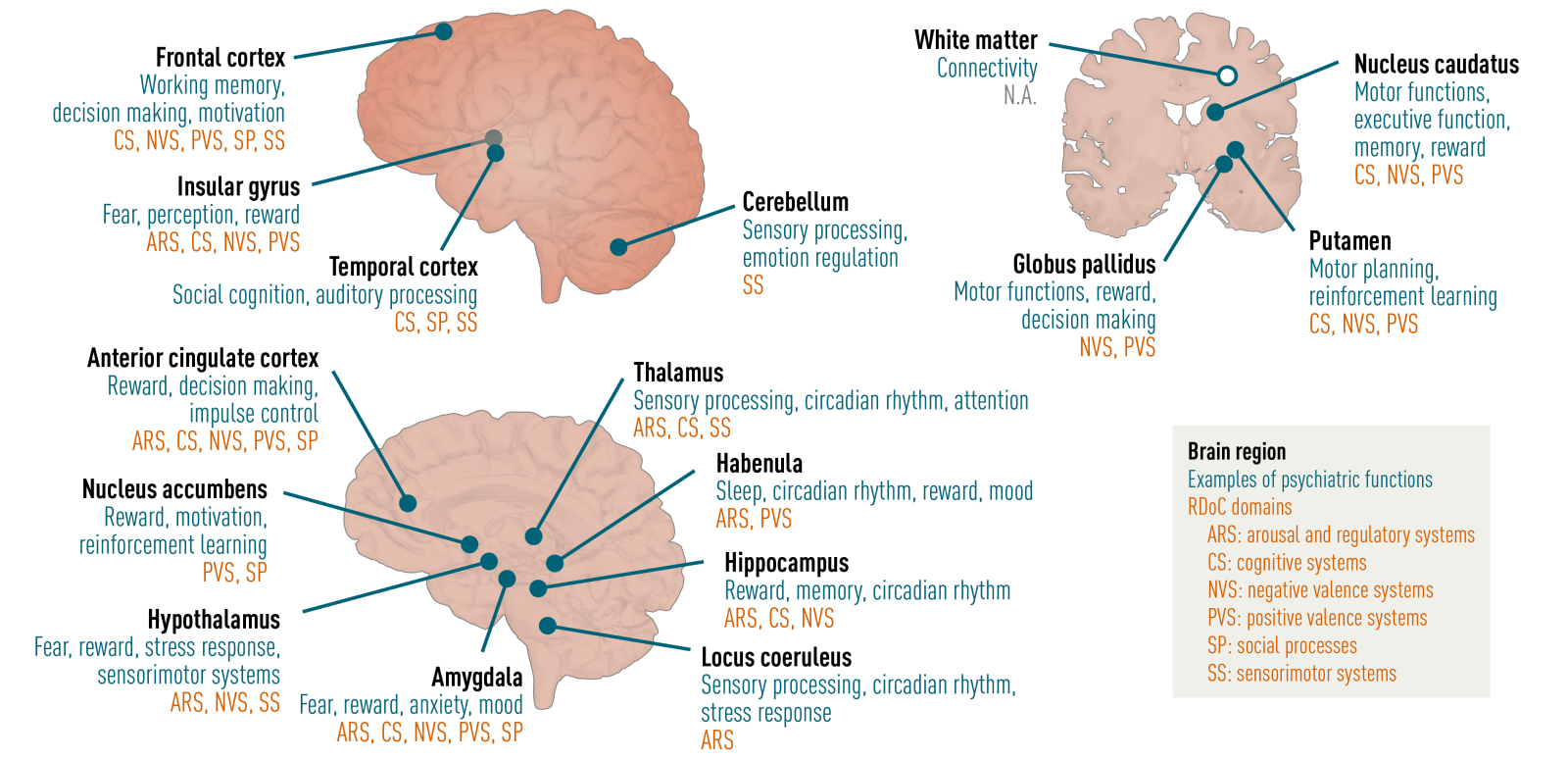
Het doel van werkpakket 2 is het creëren van een moleculaire menselijke hersenatlas met een focus op hersengebieden geassocieerd met psychiatrische symptomen door middel van een multi-omics benadering. Deze omvatten spatial transcriptomics, chemische proteomics en metabolomics, op cel-resolutie van hersengebieden over meerdere neuropsychiatrische stoornissen.
De komst van verschillende revolutionaire en krachtige nieuwe technologieën in de moleculaire biologie en scheikunde, zoals single cell transcriptomics, spatial transcriptomics met hoge resolutie, (chemische) proteomics en geavanceerde microscopiemethoden, stelt ons in staat niet alleen potentiële veranderingen in genactiviteit te bestuderen, maar ook de spatiotemporele veranderingen en functie van eiwitten in postmortem menselijke hersenen op nanoschaal. Met behulp van deze hulpmiddelen willen we een moleculaire atlas van het menselijk brein op subcellulaire schaal construeren met de bedoeling de moleculaire processen af te bakenen die ten grondslag liggen aan de veranderingen in het netwerk en de cel-cel interacties bij psychiatrische stoornissen.
We zullen een multiregionale moleculaire atlas van NBB-donoren genereren met uitgebreide klinische fenotypes en de diepgaande fenotypering van moleculaire en cellulaire kenmerken geassocieerd met geselecteerde fenotypes in specifieke hersengebieden. We zullen inzoomen op neuron-glia-interacties om afwijkende cel-cel-interacties en communicatie bij psychiatrische stoornissen in kaart te brengen. De geïdentificeerde doelwitten zullen gevalideerd worden in onafhankelijke datasets en gekarakteriseerd worden op moleculair en cellulair niveau over regio’s – patiënten – weefseltypen heen.
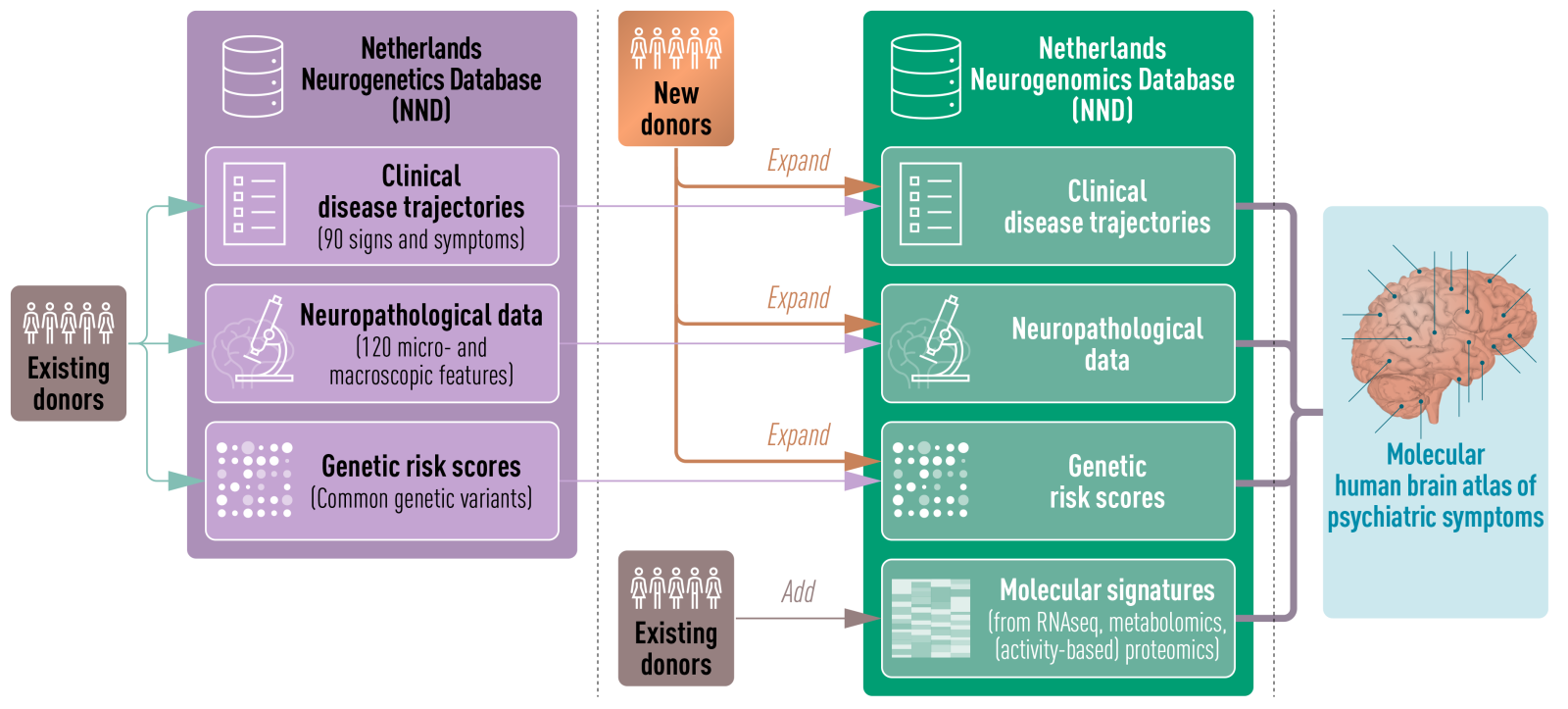
Doel-identificatie met behulp van de Nederlandse Neurogenomics Database (NND)
Leiders: Inge Holtman and Ahmed Mahfouz
Werkpakket 3 richt zich op het toepassen van geavanceerde statistische en machine learning-methoden om diverse multimodale gegevens te integreren. Het doel is om een dieper inzicht te verkrijgen in de neurobiologie van neuropsychiatrische aandoeningen en om nieuwe therapeutische doelwitten te identificeren. Binnen het iCNS-consortium worden grote verzamelingen van multimodale datasets gegenereerd. Deze omvatten genetische risicoscores, genomische profielen, chemische biologiegegevens en klinische ziekteverlopen, afkomstig van hersendonoren van de Netherlands Brain Bank. De Netherlands Neurogenomics Database (NND) speelt hierbij een cruciale rol. Het biedt een platform om monsters en datasets te volgen en ondersteunt zowel handmatige als datagestuurde curatie, wat de integratie van gegevens bevordert.
WP3 combineert deze gegevens met internationale datasets, zoals die van PsychEncode. Het doel is om neurobiologische mechanismen en celtype-interactienetwerken te identificeren die ten grondslag liggen aan ziekteprogressie. Voorspelde doelwitten zullen vervolgens in andere werkpakketten verder worden onderzocht. Daarnaast ondersteunt de NND voorspellende modellering van neuropathologieën, evenals de identificatie van moleculaire en klinische endofenotypen ter verbetering van diagnostische nauwkeurigheid. Dankzij geavanceerde computationele methoden zal WP3 unieke analyses van neuron-glia-interacties over verschillende hersenaandoeningen mogelijk maken. De open toegankelijkheid van de NND maakt het een waardevolle bron voor onderzoekers wereldwijd, gericht op innovatieve neurogenomische analyses.
Ontwikkeling van chemische probes en methoden voor de moleculaire menselijke hersenatlas en targetvalidatie
Leider: Sander van Kasteren
Werkpakket 4 is gericht op het bieden van nieuwe chemische benaderingen die het mogelijk maken hersenmonsters te bestuderen op een manier die verder gaat dan DNA en RNA. De ruimtelijke analyse en visualisatie van bepaalde enzymactiviteiten in de hersenen, zoals de enzymen die betrokken zijn bij de productie en afbraak van neuro-actieve liganden. De reden hiervoor is dat enzymactiviteiten en mRNA-niveaus voor deze eiwitten zeer slecht correleren in de hersenen en daarom is deze feitelijke activiteitsinformatie nodig over hoe enzymen de functie beïnvloeden.
WP4 richt zich ook op het ontwikkelen van tools om eiwitniveaus te manipuleren in het primaire menselijke brein. De uitdaging hierbij is dat het primair menselijk weefsel is, wat betekent dat knock-outtechnologie niet compatibel is met deze aanpak. In plaats daarvan zullen we daarom nieuwe chemische mutagenese- en knock-outmethoden ontwikkelen. Verder zullen nieuwe methoden en reagentia worden ontwikkeld om de interactie tussen cellen in de hersenen te bekijken. Een van de belangrijkste hypotheses van het voorstel is dat de interactie tussen verschillende celtypes in de hersenen ontregeld is, wat leidt tot ziekte. De studie van dit fenomeen vereist nieuwe benaderingen om deze interacties tot op atomair niveau in beeld te brengen, die we hier zullen ontwikkelen. De laatste set nieuwe methoden die we hebben ontwikkeld is het in beeld brengen van de stromen van voedingsstoffen en andere kleine moleculen door de hersenen. Dit zal helpen om enkele andere manieren te begrijpen waarop de verschillende cellen in de hersenen elkaar beïnvloeden.
Om deze nieuwe technologieën succesvol te implementeren zullen de WP4 onderzoekers nauw samenwerken met andere werkpakketten om ervoor te zorgen dat de reagentia allemaal compatibel zijn met de experimentele systemen en modellen die gebruikt worden in het bredere voorstel. Alle projecten zullen daarom worden gekoppeld aan projecten van biologische onderzoekers.
Targetvalidatie in geavanceerde modelsystemen
Leiders: Aniko Korosi & Femke de Vrij
Werkpakket 5 heeft tot doel mechanistisch, causaal en functioneel inzicht te verschaffen in nieuwe moleculaire mechanismes die aan psychiatrische symptomatologie ten grondslag liggen. Met de projecten in WP5 zal een onderzoekslijn worden opgezet om met name neuron-glia interacties in vitro en in vivo te bestuderen om mechanistisch, causaal en functioneel inzicht te bieden in de functie en rol van nieuw geïdentificeerde moleculen bij psychiatrische symptomatologie. Ook zullen kandidaat target moleculen worden getest voor innovatieve therapeutische toepassingen bij neuropsychiatrische stoornissen.
We zullen vernieuwende benaderingen toepassen zoals glia-specifieke virale tools en state-of-the-art chemie ontwikkelen in samenwerking met WP4 onderzoekers. Met deze benaderingen kunnen neuron-glia interacties op hogere resolutie ex vivo gevisualiseerd en gekarakteriseerd worden. De moleculaire veranderingen zullen vervolgens worden gemanipuleerd in zowel muismodellen, als ook in platforms van humaan geïnduceerde pluripotente stamcel (hiPSC)-afgeleide kweken en zogenaamde hersenorganoïden. In de muismodellen zullen WP5 onderzoekers ook targets valideren en proof-of-concept interventiestudies uitvoeren. Het werk zal variëren van analyses van cellulaire, elektrofysiologische eigenschappen in neurale netwerken in vitro, tot gedragsscreening met in vivo diermodellen. Het uiteindelijke doel is de causaliteit, cellulaire specificiteit en verbanden tussen eiwitdysfunctie en veranderingen in gedrag en cognitie in neuropsychiatrische aandoeningen beter te begrijpen.
.jpg)
